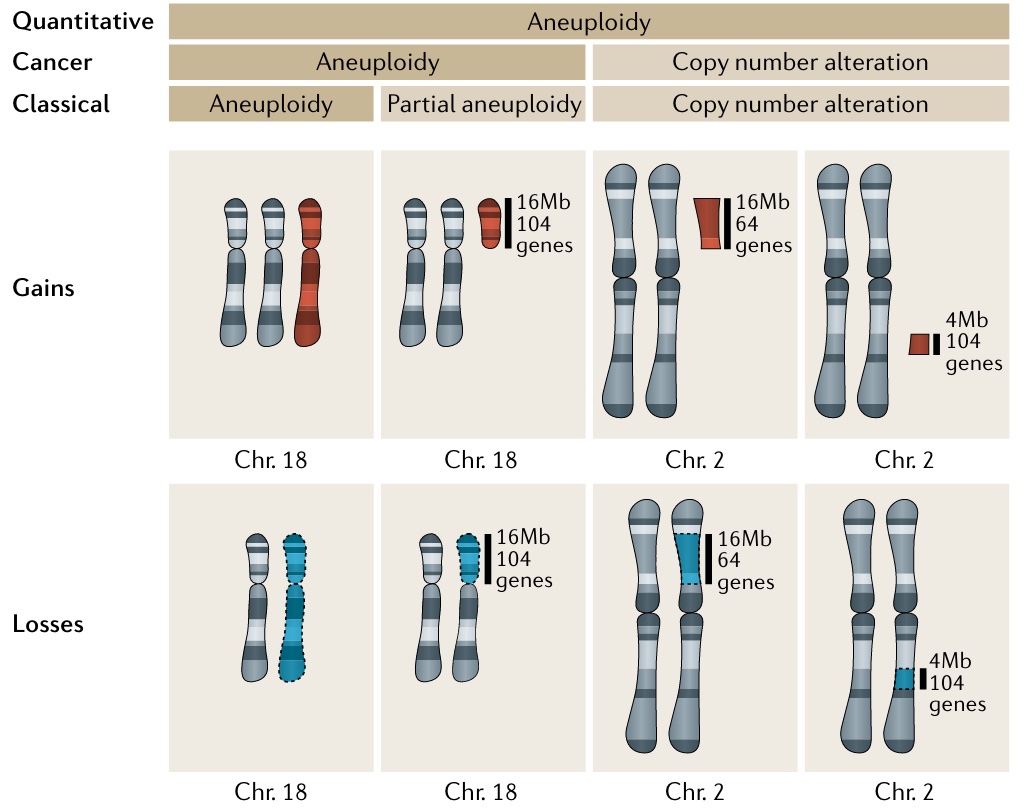
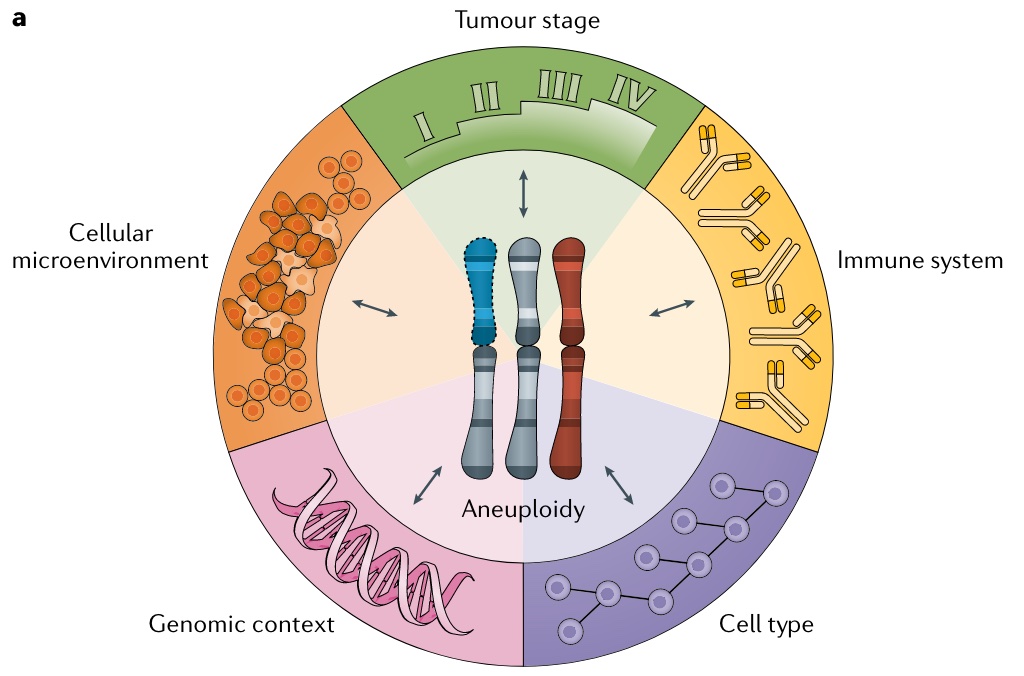
同一天在 Nature Cancer 和 Nature Genetics 发表两篇文章是一种什么体验?今天我们用一天发表两篇文献解读从侧面体会下 😃 故事要从2022年9月9日说起。因为我最近一年多比较关注肿瘤基因组不稳定性相关临床研究进展,于是会留意一些该领域内活跃大佬的动态。 今年9月9号,我发现来自芝加哥大学的Liam Flinn Spurr(2021年他曾在Bioinformatics发表过肿瘤非整倍体分析的方法学文章)说自己有三篇一作文章在一周之内同时被Nature Cancer、Nature Genetic 和 NPJ journal 接受。 等文章online,这一等就是三个月。 11月28日,他作为第一作者在 Nature Cancer 的文章正式 online,作者通过一项临床研究发现高度非整倍体的非小细胞肺癌对放疗联合免疫治疗更敏感。同时在Nature Genetics online 的文章则介绍了在低TMB患者中可以通过肿瘤非整倍体程度预测泛癌的免疫治疗疗效。 今天的推送我们一起了解第一篇文章的相关内容,万一对你有点启发呢。 基因组不稳定性是肿瘤 hallmarks 之一,从泛尺度来说,包括碱基 / 基因层面、染色体片段、染色体臂水平和染色体水平的扩增和缺失。如下图所示,我们常说的非整倍体(aneuplooidy)程度就是特指肿瘤细胞染色体臂和染色体层面的扩增缺失现象。 关于非整倍体这类基因组不稳定性对于肿瘤的影响已经有了不同维度的很多研究,不同的肿瘤分期和组织细胞类型会有不同非整倍体特征,非整倍体程度也会对肿瘤免疫系统、肿瘤微环境和基因组变异产生影响。 先来看看第一篇文章。 联合放疗(RT)和免疫检查点抑制剂(ICB)治疗癌症的临床实验有超过500多项目,然而大多数试验并没有发现积极的相互作用。 目前,一个关键的临床问题是我们是否以及该如何将RT和ICB结合起来以改善患者的预后。此外相关的生物标志物也将有助于选择最有可能从联合治疗中受益的患者。 PD-L1表达、肿瘤突变负荷(TMB)、效应T细胞和肿瘤新抗原的数量等等已经被证明可以预测抗PD-1或者抗CTLA-4的应答。然而,这些生物标志物或者是否有其它更好的生物标志物中可以预测RT和ICB的联合治疗效果也尚不清楚。 作者团队进行了一项随机临床试验,旨在针对未经选择的转移性非小细胞肺癌患者,评估ICB联合多部位消融体部放疗的一线治疗安全性和有效性。本文作为该试验的二次分析,分析了治疗前和治疗中匹配样本的肿瘤活检分子特征,以展示放射治疗和ICB时机对肿瘤免疫基因组环境的影响。 具体的实验设计如下图所示,对于转移性的非小细胞肺癌 (NSCLC) 患者,随机分为两组分别在试验中接受同步或序贯的立体定向消融体部放疗 (SBRT) 联合ipi/nivo (ICB)治疗。 具体的样本收集时间点和样本检测数据类型如下图所示,在两组患者治疗前收集样本,在1-2周的SBRT治疗后再收集一次样本。分别统计临床相关信息和并进行RNA及DNA样本检测。 因为包含RNAseq样本,就可以基于大量免疫相关的基因集通过ssGSEA和差异表达分析等方法,比较两种不同治疗方式前后免疫相关的变化。比如作者研究发现,SBRT + ICB 的联合治疗导致参与抗原呈递、干扰素应答、细胞因子和趋化因子信号传导以及效应 T 细胞功能的基因上调。相反,SBRT 则抑制了细胞毒性T细胞相关基因的表达。 因为这部分相关内容不是我们今天要讨论的重点,如果感兴趣可以阅读原文。 在进行了免疫微环境相关的比较之后,我们自然会关心 ICB 反应的那些生物标志物是否可以用来预测RT + ICB 的响应效果。通过分析发现 T 细胞信号、 TMB、新抗原负荷和 PD-L1表达这些指标都没有表现出预测价值。然而,更高的非整倍体评分确预示着序贯治疗(而非同步治疗)的不良预后。 使用肿瘤纯度变化作为局部反应的替代指标,研究发现在SBRT治疗前的非整倍体评分和肿瘤纯度变化之间没有相关性,但是在同步治疗组内,两者之间的相关性非常强。提示SBRT+ipi/nivo比SBRT 能更有效地消除高度非整倍体肿瘤。 作者进一步研究了非整倍体评分和生存之间的关系。发现呈高度非整倍体的肿瘤(非整倍体评分≥队列中位数)的患者,与序贯治疗相比同步治疗可提高生存率。相反在非整倍体程度较低的肿瘤患者中没有观察到这种关系。 对于同步放疗联合ICB治疗有利于高度非整倍体的患者这一假设,作者研究了他们机构的另外一个58名转移性非小细胞肺癌患者的独立临床队列。 这些患者部分接受单独的ICB治疗(下图实线蓝色),部分接受了放疗和ICB的联合治疗(下图实线橙色),这部分患者这部分采用了同步治疗(下图虚线紫色)部分采用了序贯治疗(虚线黄色)。且该队列的临床和病理因素和之前的队列是平衡的。 与之前的假设一致,对于高非整倍体评分的患者(评分大于队列中位数),可以发现单独使用ICB的效果要显著差于RT+ICB的联合治疗,且在接受RT+ICB的患者中,同步治疗的患者比序贯治疗的患者预后更好(尽管这没有达到统计学意义)。但是相比之下,在非整倍体评分较低的肿瘤患者中,ICB中加入RT并没有改善患者的疗效。 至此,针对该队列的二次分析基本就完成了。我们可以看到,虽然是两个小队列,且验证队列的治疗方式并不是非常规整(其实有能用的验证队列已经很不容易了),但配合上有明确临床价值的分析结果以及包含了DNA和RNA两个维度丰富的分析内容,依旧可以发表在Nature Cancer这样的顶级期刊。 又是基于验证队列的分析结果,我们很自然的也会产生一个疑问:非整倍体的评分是否可以推广到仅有ICB治疗的患者中。 有趣的事,在一组来自MSKCC包括了350名接受了ICB治疗的NSCLC患者中,多因素Cox分析发现TMB和非整倍体评分均可以对立的预测OS。 将患者按TMB的中位数进行划分,高TMB患者中,不同程度的非整倍体无法区分出患者的预后;但是在低TMB的患者中,高非整倍体评分的患者预后要显著的比低非整倍体评分的患者更差。 进一步支持了将高非整倍体评分作为转移性非小细胞肺癌ICB反应的生物标志物实用性。 也正是因为最后这一小部分的研究,衍生出了同一天发表在Nature genetics的另一个文章。关于这篇文章的细节,我们下一篇博客再见~ 本文作者:思考问题的熊 版权声明:本博客所有文章除特别声明外,均采用 知识共享署名-非商业性使用-禁止演绎 4.0 国际许可协议 (CC BY-NC-ND 4.0) 进行许可。 如果你对这篇文章感兴趣,欢迎通过邮箱订阅我的 「熊言熊语」会员通讯,我将第一时间与你分享肿瘤生物医药领域最新行业研究进展和我的所思所学所想,点此链接即可进行免费订阅。写在前面
关于肿瘤非整倍体
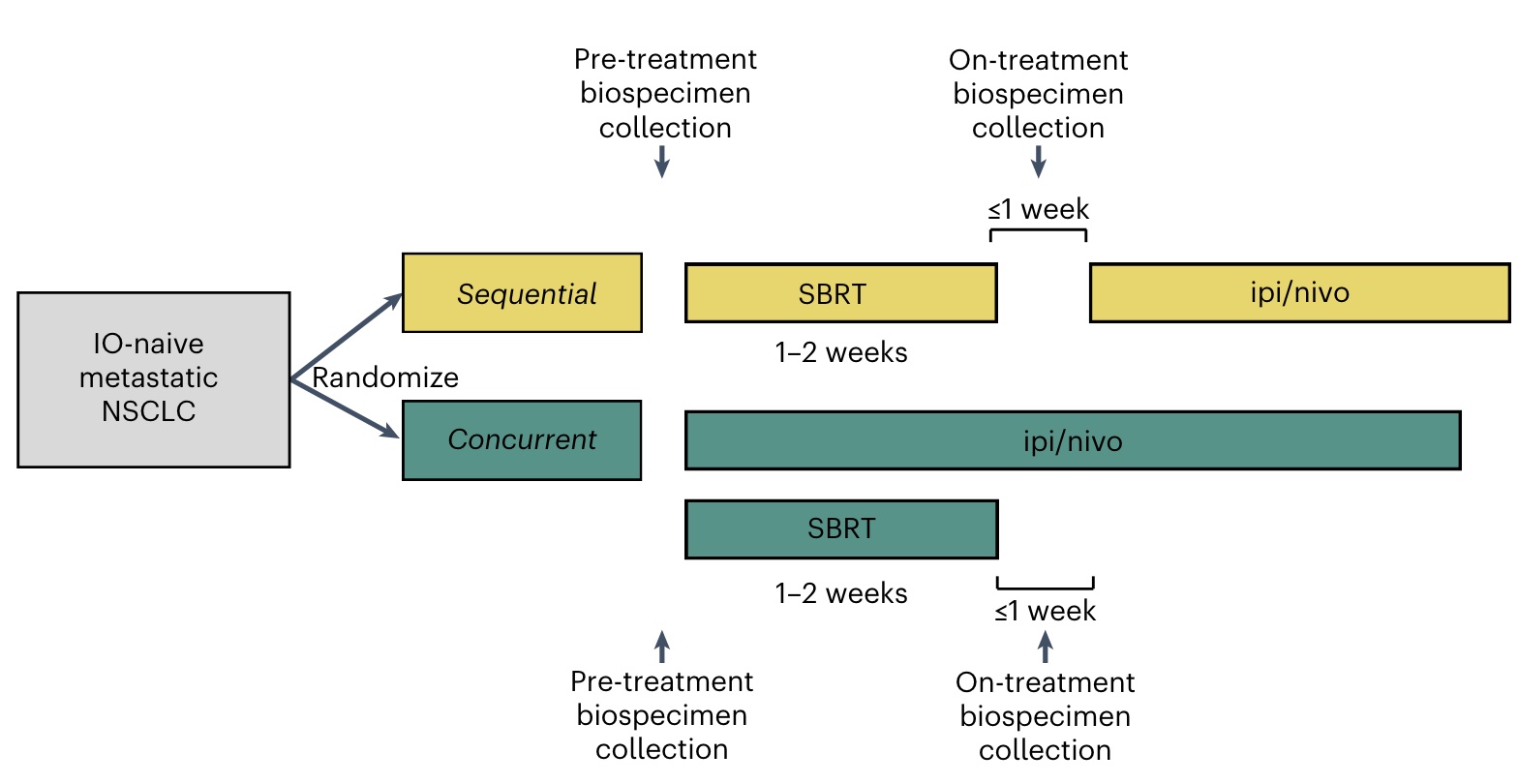
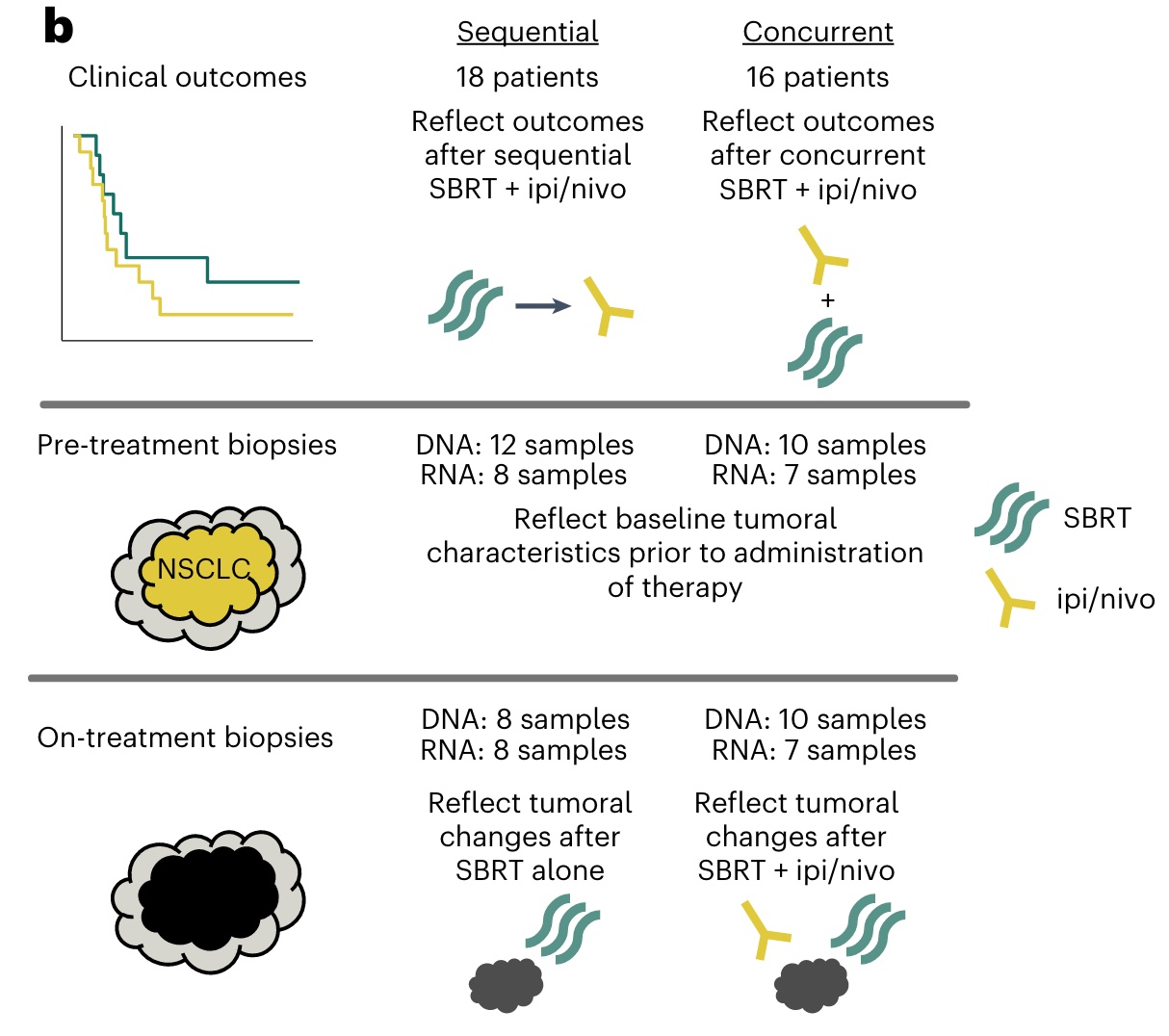
高度非整倍体非小细胞肺癌对于放疗联合免疫治疗更敏感


· 分享链接 https://kaopubear.top/blog/2022-12-01-highly-aneuploid-nsclc-rt-icb/