本文为熊言熊语邮件通讯会员计划内容的试读版,完整内容请点击通讯主页订阅并查看。 你好,我是思考问题的熊,本内容是参加会员计划读者的专属内容,感谢你通过会员计划支持我持续创作。展信佳~ 本期内容: 今天这一期内容(part1),你将会阅读到 HRD/DDR 生物学背景、临床应用场景和临床验证历程的前半部分内容(2010-2016年),全文接近5000字。 下期预告: Part2中,你会阅读到HRD临床验证历程的后半部分内容(2016-2020年) 同源重组修复缺陷(homologous recombination deficiency, HRD)我们在 V012plus.熊言熊语:从靶向治疗耐药机制到联合用药策略 介绍靶向治疗核心原理中合成致死的时候就埋下了一个引子。 了解同源重组修复缺陷的前提是明白何为同源重组修复(homologous recombination repair, HRR),而明白 HRR 需要从其更上游的概念 DNA 损伤修复(DNA damage repair, DDR)开始。 只要用 DNA damage repair/response + cancer 去检索,你就可以看到不少综述,以下是部分综述的 DDR 通路图供你赏析。 如果你想了解相对全面的通路,不妨参考 cellsignal 网站的整理版本。 如果你想参考相对清晰简洁的示意图,可以理解下面这个示意图。 简单说,不同的 DNA 损伤类型可以通过不同的方式进行修复。 比如,含有错配核苷酸的 DNA 复制错误可以通过错配修复(DNA mismatch repair, MMR)途径进行修复(在 TMB 对应的文章中我们会进一步展开);针对 DNA 损伤常见的单链断裂(single-strand break, SSB)或者对双螺旋结构影响较小的损伤等,可以通过碱基切除修复(base excision repair, BER);针对双链损伤(DSB),则有多种不同的修复方法。 其中,HRR 是负责修复 DSB 与 DNA 链间交联(interstrand crosslinks)最为准确且高保真的 DNA 损伤修复系统(依赖 DNA 模板);而非同源末端连接(non-homologous end joining,NHEJ)、微同源末端连接(microhomology mediated end joining,MMEJ)和单链退火途径 (single-strand annealing,SSA)这些属于低保真高易错的损伤修复途径(可以理解为稀里糊涂先把断了的接上,不管原先是什么样子)。 如果细胞的 HRR 功能出现问题(HRD),细胞就不得不调用那些低保真的修复方案,产生各种大片段的缺失插入,拷贝数异常等现象,进而造成细胞染色体和基因组的极度不稳定。 造成 HRD 的原因很复杂而且目前也没有完全研究清楚。一方面 HR 过程中主要涉及到 BRCA1/2,RAD51,以及 BRCA2 定位基因 (PALB2) 等基因突变;另一方面,研究人员还发现像 BRCA 基因的表观遗传甲基化失活也可以导致 HRD。 在上一部分我们提到 HRD 的出现会使得细胞依赖低保真的方案进行 DNA 修复,而基于此出现的基因组不稳定则又是癌症的 Hallmarks 之一。(HRD 是造成基因组不稳定性的重要原因之一) 因为 HRR 在 DNA 双链修复上的重要功能,如果一个细胞发生了 HRD 同时人为让其单链修复出现问题,就会触发「合成致死」效应,让癌细胞的 DNA 修复系统就会被破坏进而死亡;另外一方面,HRD 会让肿瘤细胞对能诱发 DNA 交联的含铂化疗药物更加敏感。 基于以上基础原理,HRD 自然就有可能作为一个生物标志物,在铂化疗和抑制单链修复的PARP 抑制剂治疗中发挥临床作用。 虽然原理如此,HRD 究竟能在什么癌种的什么条件下指导治疗,直到目前都还存在很多疑问,而已经获批的临床场景验证也经历了非常漫长的过程。 HRD 作为生物标志物的验证史可以说就是 PARPi 适应症的发展史。 需要说明的是,因为 PARPi 目前在包括卵巢癌、乳腺癌和胰腺癌等多个癌种中均有临床应用,为了更好的梳理 HRD 作为生物标志物的提出和临床验证历程,这一部分我们仅选取一种 HRD 计算方法(GIS)在卵巢癌单一癌种的应用进行展开。 关于 HRD 的更多评价计算方法和 HRD 在非卵巢癌中的应用场景,我们会在后续的「方法和产品」以及「前景和思考」部分有所涉及。 PARP 全称是 Poly (ADP-ribose) polymerase,PARP 蛋白家族涉及包括 DNA 修复、基因组稳定性和细胞程序性死亡在内的诸多细胞生物学过程。 2009 年的 ASCO 大会,研究人员分享了一类新型靶向药物令人鼓舞的研究发现,代号为 AZD2281 的药物适用于那些涉及到 BRCA 基因突变的卵巢癌。这类药物就是如今我们所知的 PARPi,而 AZD2281 的中文名字就是如今应用很广泛的奥拉帕利(Olaparib)。 PARP 抑制剂旨在使癌细胞用于修复 DNA 损伤的关键酶失效并促使癌细胞死亡,还可能使癌细胞对其他治疗如化疗药物更加敏感。 当然,彼时还需要进一步长期随机临床试验来确定 PARP 抑制剂是否真正有益于卵巢癌患者,如果是的话,哪些特定类型的卵巢癌最有可能对该药物产生反应?其它癌种效果如何? 这些都是以后的故事。 陆陆续续,三种 PARPis:奥拉帕利(Olaparib),鲁卡帕利(Rucaparib),尼拉帕利(Niraparib) 早期相继被 FDA 批准用于具有胚系 BRCA 突变的卵巢癌患者。 然而,后续越来越多的研究发现仅仅检测胚系或体细 BRCA 突变会低估甚至错误地鉴别可能受益于 PARPi 治疗患者,于是又把对铂类药物的敏感性也用作 HRD 的提示用来选择预期对 PARPi 敏感的患者。但是铂类药物的耐药机制也超出了 BRCA1/2 状态还是可能低估 PARPi 获益患者。 那是否有什么更好用的指标来提示HRD进而指导 PARPi的用药呢?说来话长,接下来我们需要回到2010年,从一篇方法学文章开始聊起。 🍺🍺试读结束🍺🍺 剩余内容是参加会员计划读者的专属内容 欢迎你通过会员计划支持我持续创作 如果你对这篇文章感兴趣,欢迎通过邮箱订阅我的 「熊言熊语」会员通讯,我将第一时间与你分享肿瘤生物医药领域最新行业研究进展和我的所思所学所想,点此链接即可进行免费订阅。
写在前面
生物学背景
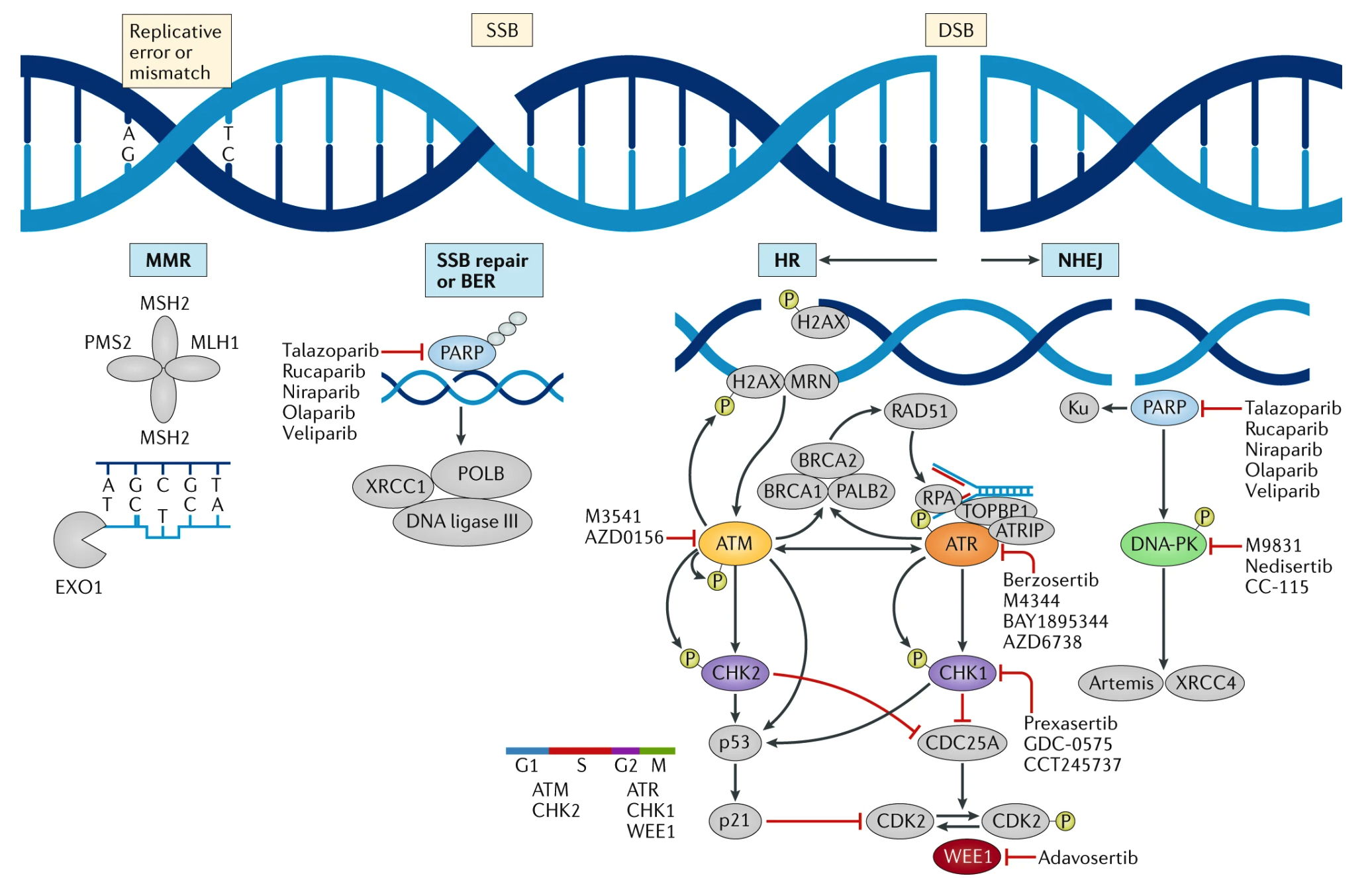
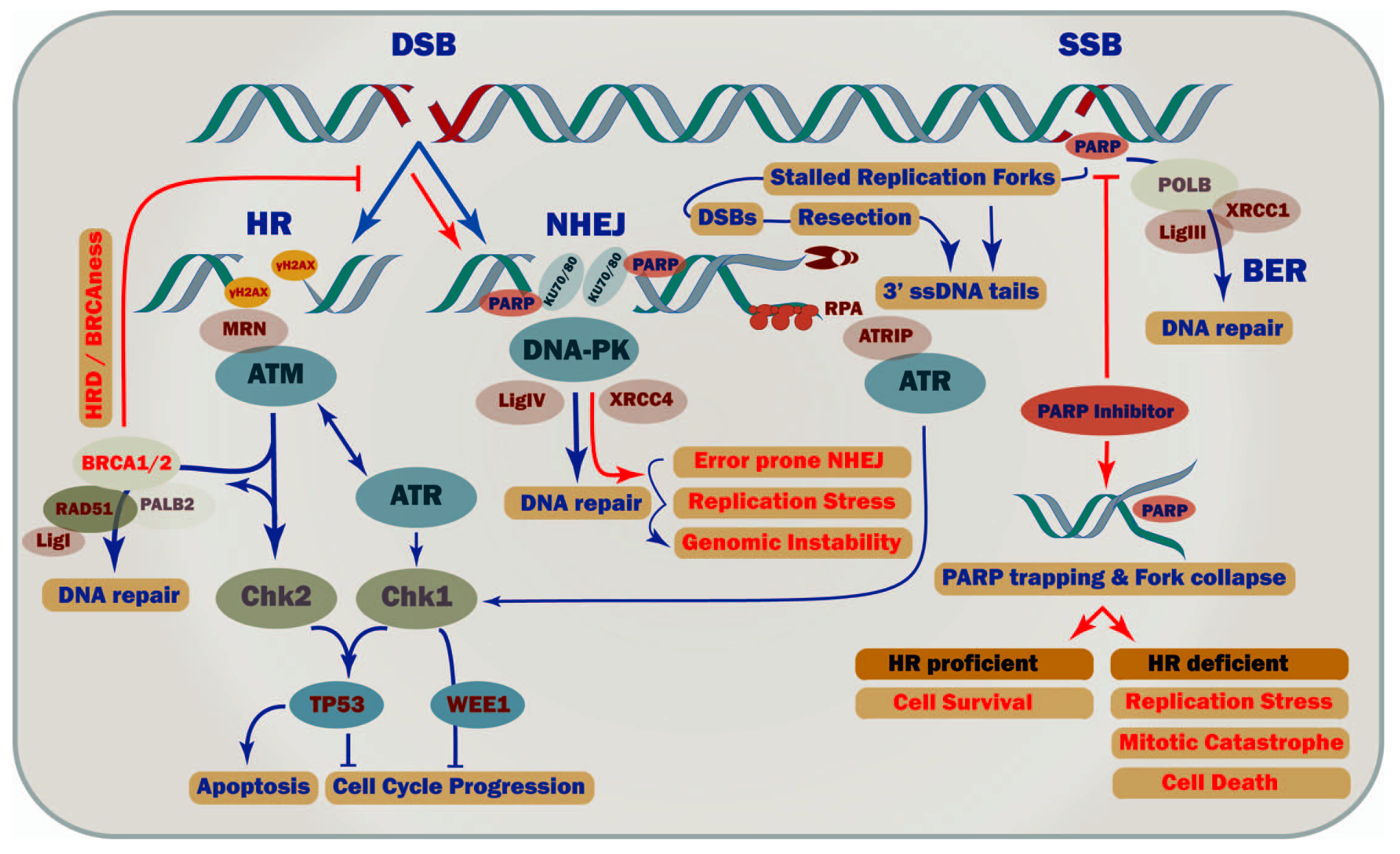
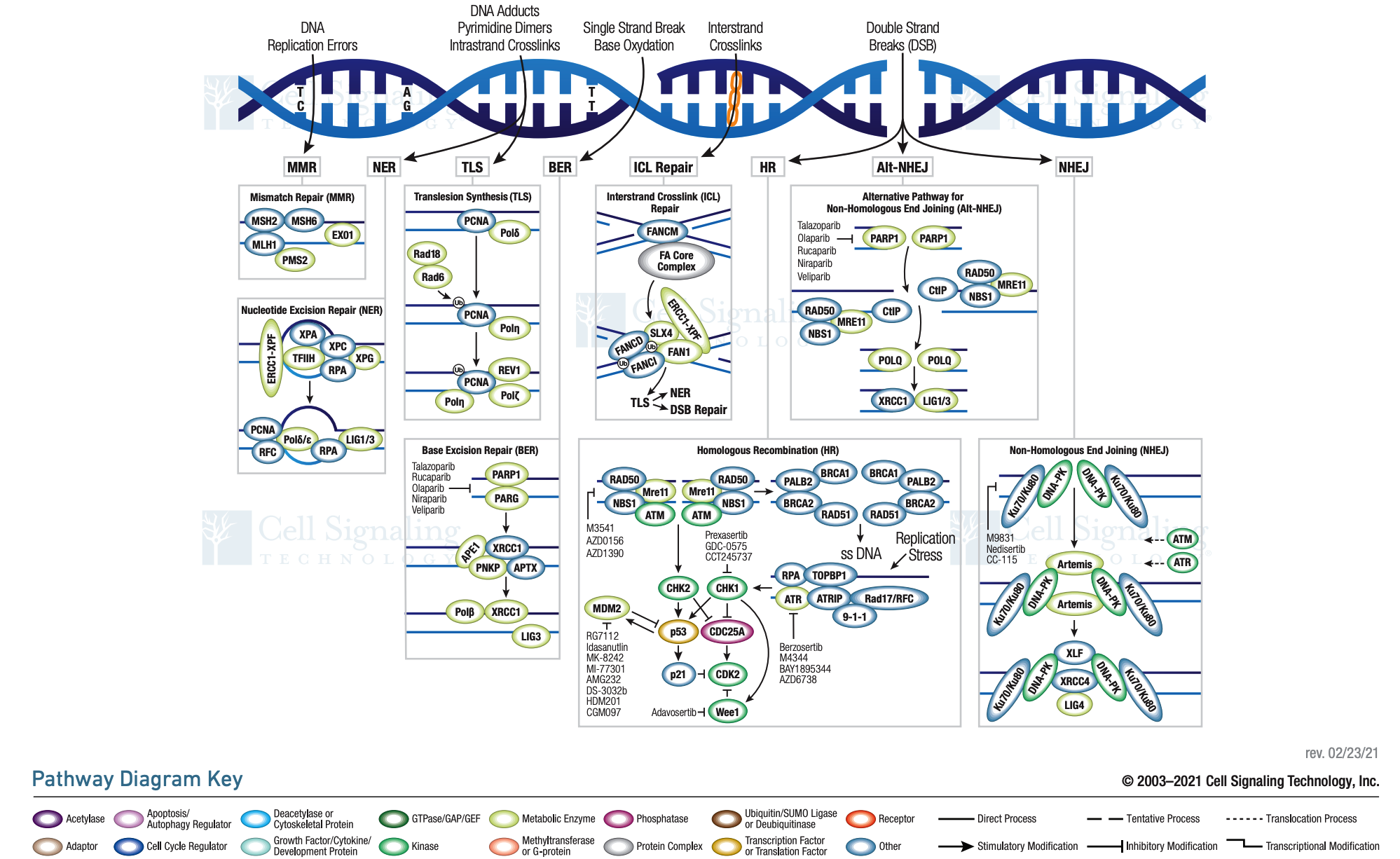
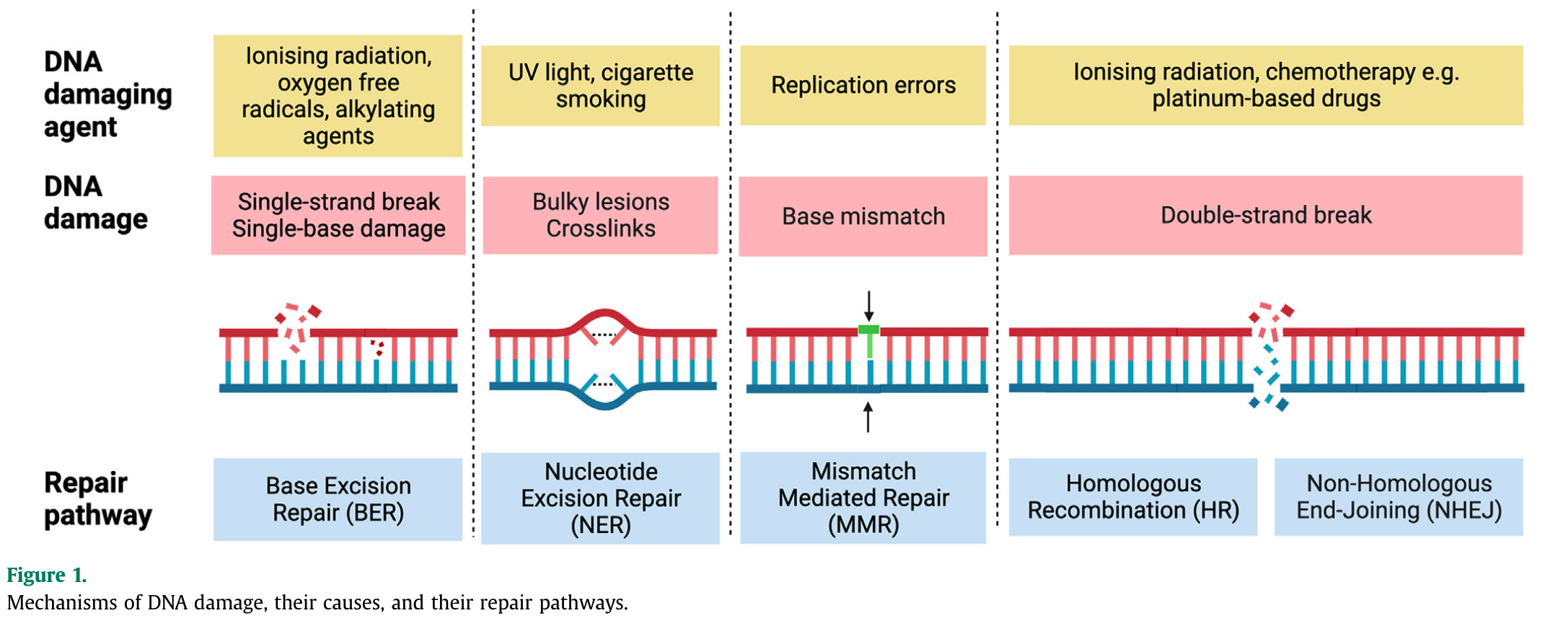
临床应用场景
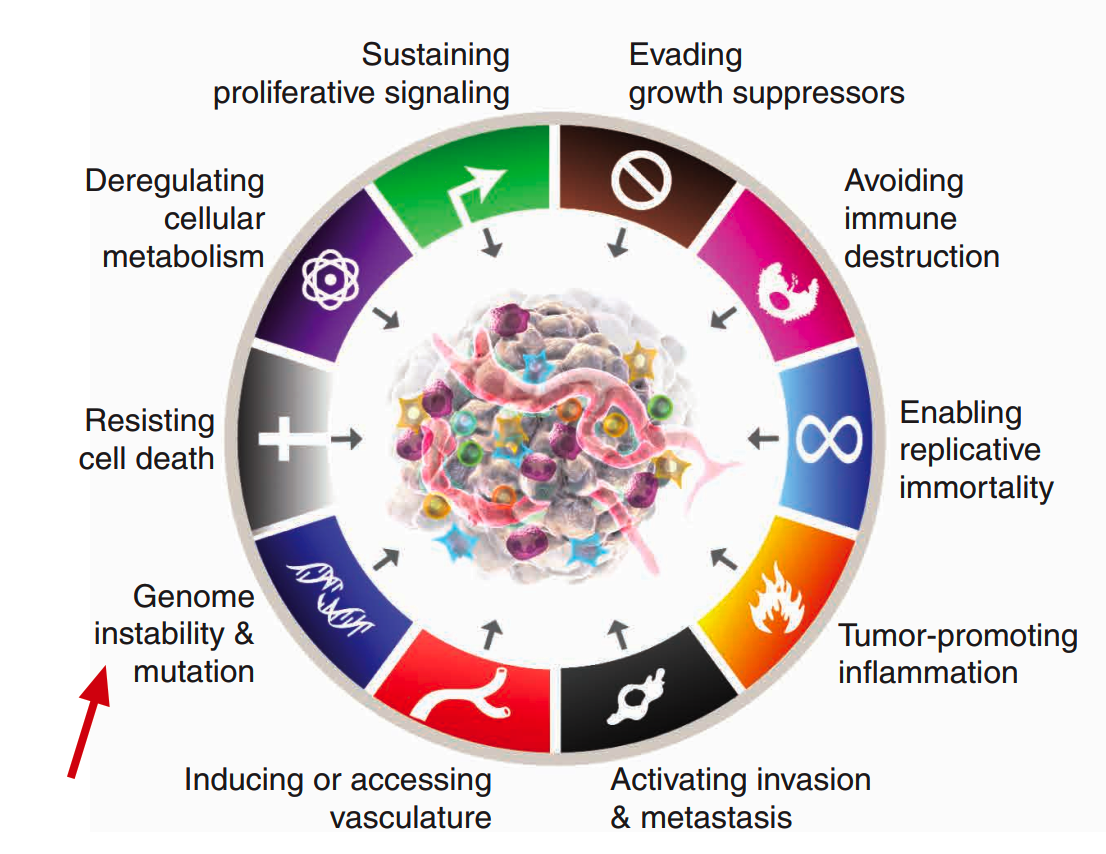
尤其是包括乳腺癌、卵巢癌、胰腺癌和前列腺癌在内的这四个癌种中,研究发现 HRD(BRCA 等基因突变)发生的频率很高,这四个癌种也因此被称作 BRCA assocatied cancer。
临床验证历程
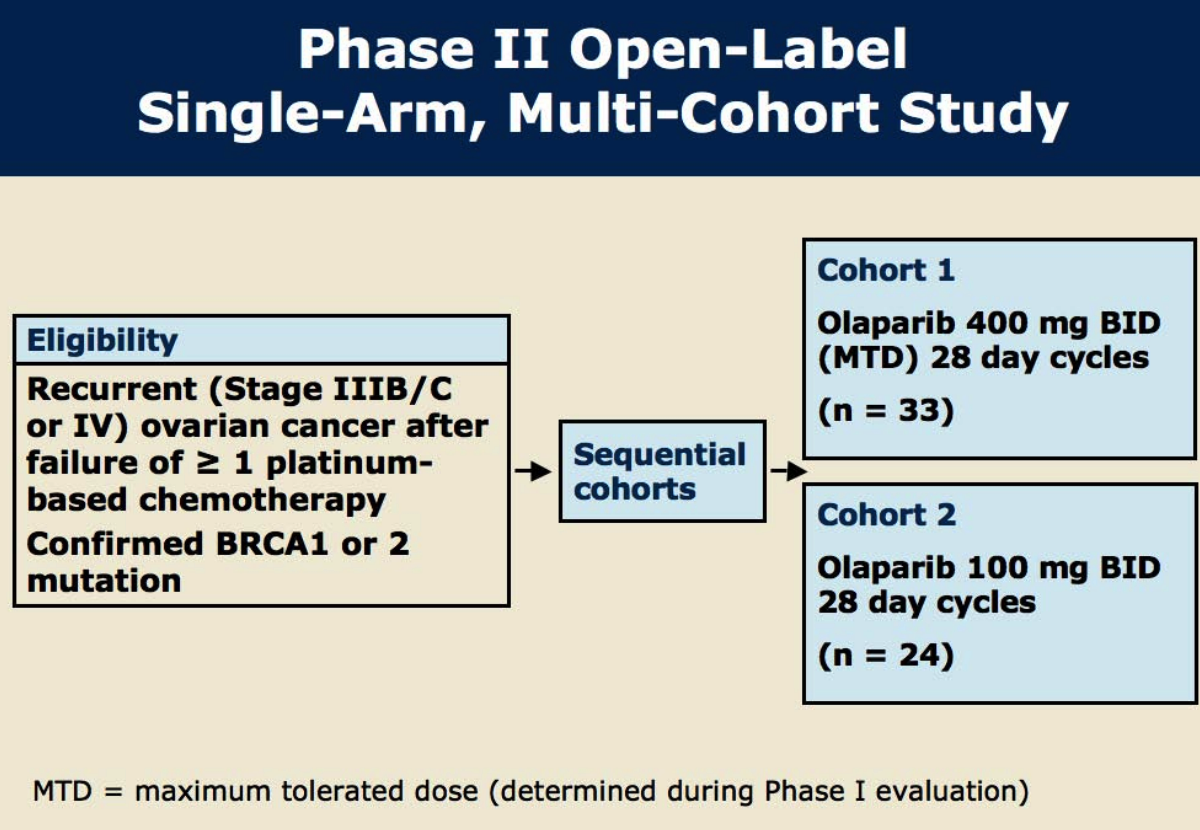
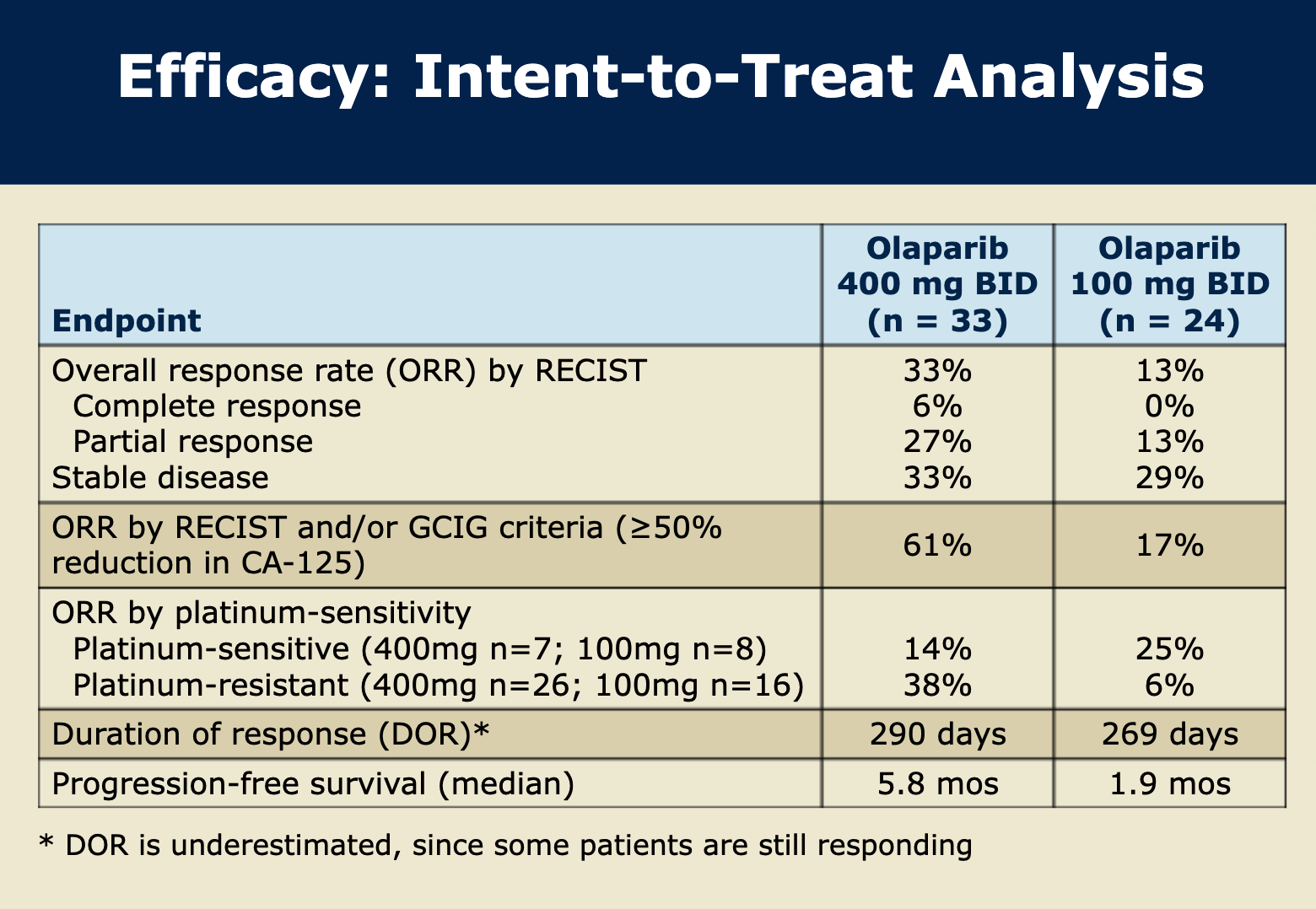
PARP 抑制剂效果初现


· 分享链接 https://kaopubear.top/blog/2023-05-03-cancer-homologous-recombination-deficiency-part1/