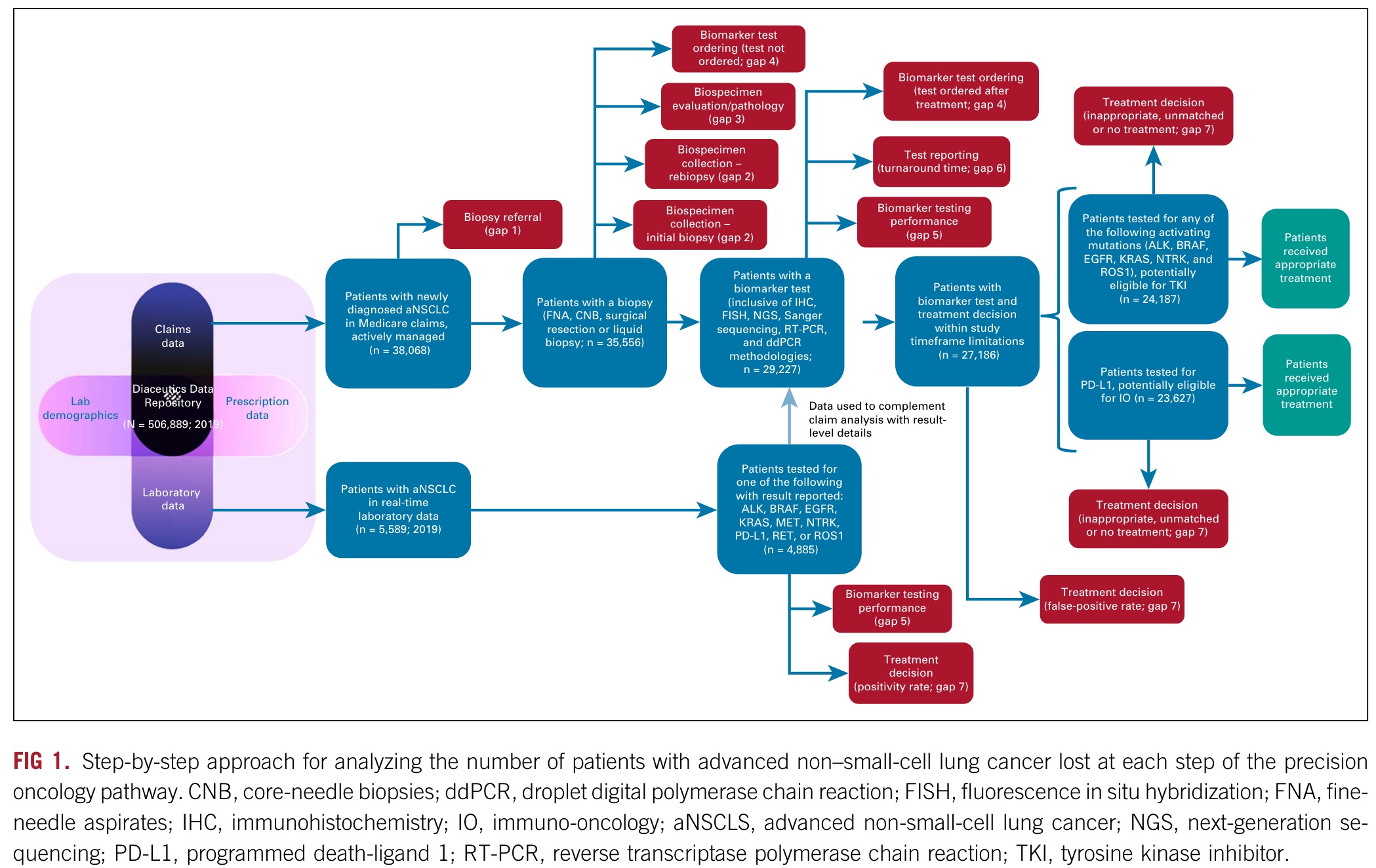
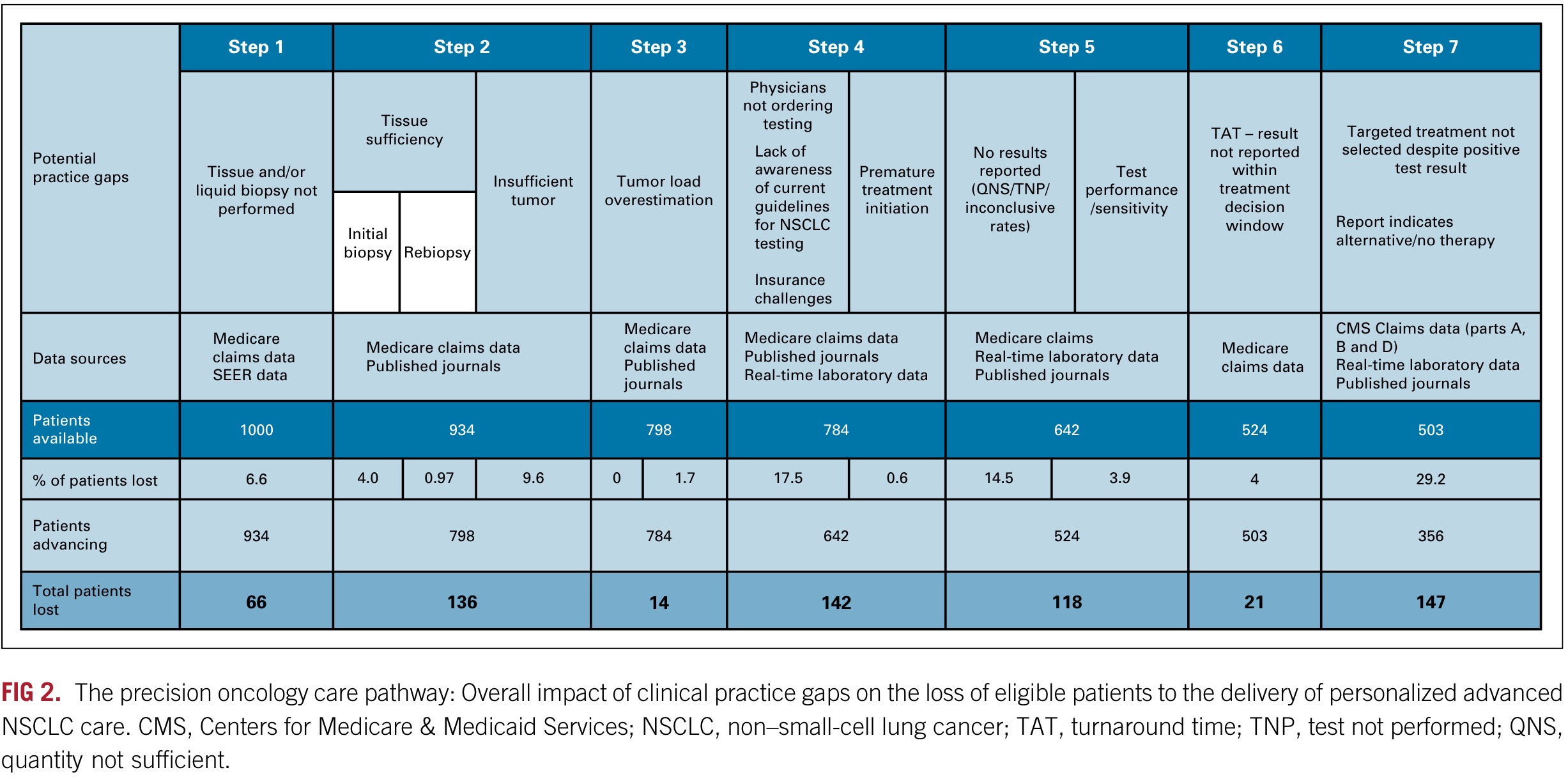
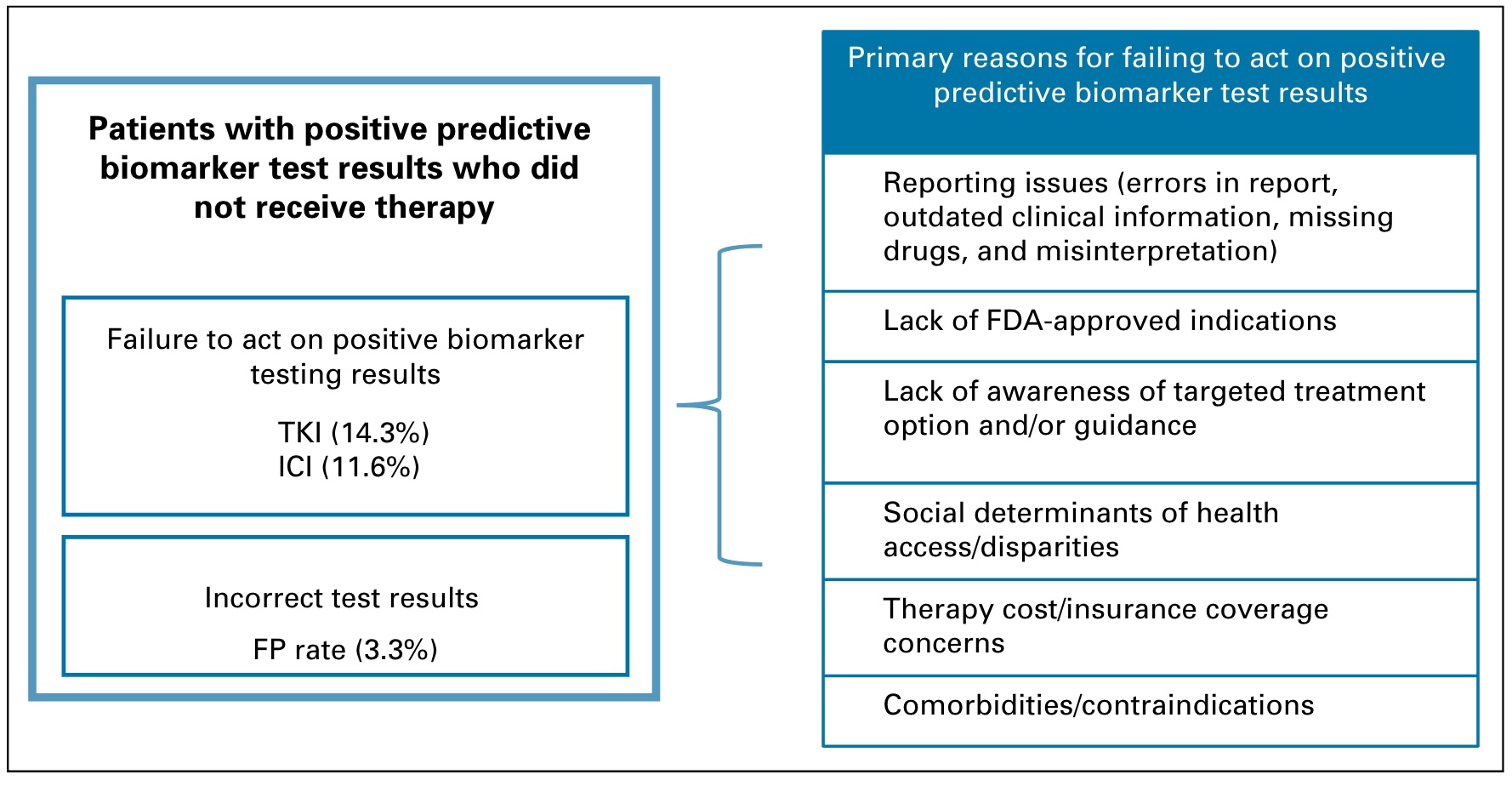
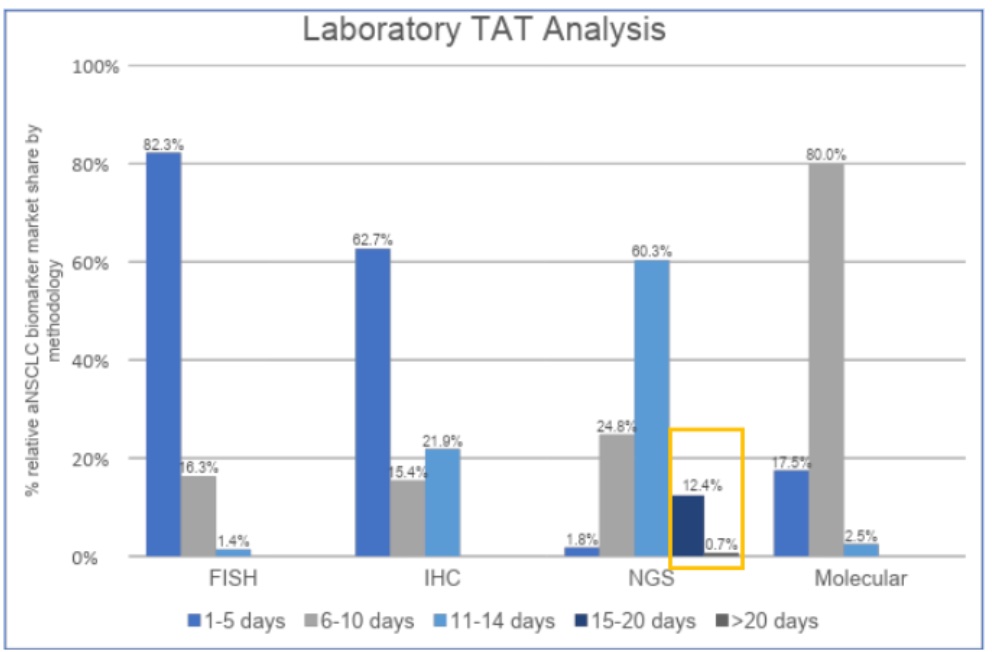
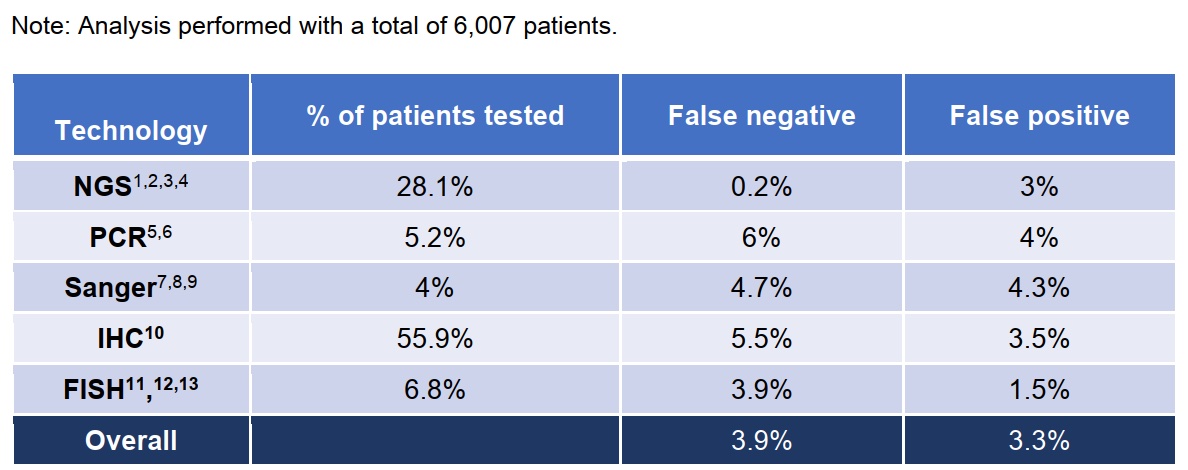
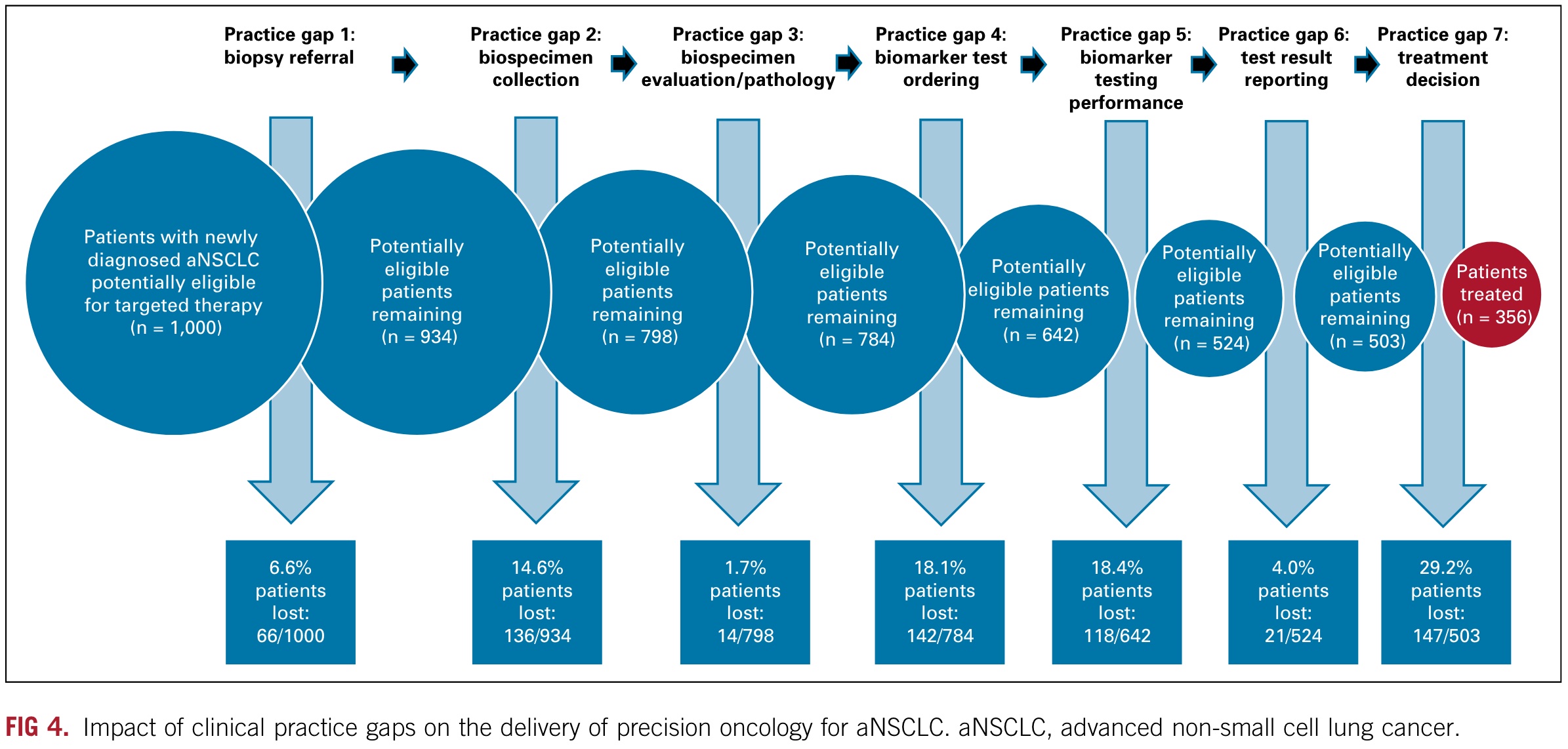
换句话,除了「贵」,还有哪些因素影响了癌症精准治疗在临床实践中的应用呢? 今年过年发生的一段对话如下: 👨:小伙子,哪里发财? 过年回来,这段对话我一直忘不掉,除了不知道该如何发财,还好奇一个问题:这么多上下游公司,有药企有诊断,这么多做科研、做研发、做销售的从业者,吭哧吭哧这么多年,究竟有多少患者从中受益,应该从哪里找问题? 换句话,除了闭眼能想到的「贵」,到底有哪些因素影响了癌症精准治疗在临床实践中的应用? 前几天一查,还真找到了 2022 年 10 月发表在 JCO Precision Oncology 的一篇论文。 这篇论文以晚期非小细胞肺癌(NSCLC)为例,详细介绍了将预测生物标志物(predictive biomarker)检测整合到癌症个性化诊疗过程中面临的挑战,并量化分析了各种临床实践障碍对治疗的真实影响。 先说结论:在美国,从诊断到治疗的过程中,由于不同临床实践障碍叠加造成的患者损失,最终大约 64% 的潜在获益晚期 NSCLC 患者没有受益于适合其疾病的癌症精确治疗。 如上图所示,该研究使用的 Diaceutics 是一个来自美国超过50万名非小细胞肺癌患者数据,包括商业和医疗保险以及实验室数据在内的多来源数据库。 其研究重点放在了精准治疗过程中从诊断到治疗七个步骤出现的障碍和各自独立及累计影响。 七个步骤如下: 当将人数标准化为1000时,如下图你可以看到每一步具体存在的问题以及陆续措施治疗机会的患者人数和比例。 在上面这幅图,我们可以发现,研究者估计有29.2%的病人没有根据他们的检测结果接受适当的针对性治疗。 根据索赔数据,确定有18.5%的病人没有接受治疗。在81.5%的接受了各种治疗的患者中 9.1%只接受化疗,14.3% 接受化疗和免疫治疗,40.8% 只接受免疫治疗,16.6% 接受靶向治疗,还有 0.7% 接受其他治疗。 14.3%的肿瘤本可以使用TKI却没有接受指定的治疗。另有11.6%的患者在IHC检测基础上获得了可针对治疗的结果,但没有接受适当免疫治疗,此外估计共有3.3%的患者的检测结果不正确(假阳性)。 推测没有接受相应治疗的原因,如下图显示,可能包括:检测报告问题(报告中的错误、过时的临床和药物信息);缺乏FDA批准的适应症(医生不清楚或不愿在适应症外用药);对靶向治疗选择的认识滞后;治疗可及性;治疗成本/保险报销范围等。 如果你关注的是肿瘤NGS检测,那么有一个好消息和一个坏消息。 坏消息是turnaround time (TAT) 统计显示:在接受生物标志物检测并报告结果的29227名患者中,研究估计有4%经历了TAT延迟进而导致治疗决定没有考虑分子检测结果,在所有方法中 13.1% 的 NGS 检测 TAT 超过了14天。 好消息是,在包括 PCR Sanger IHC和FISH在内的检测手段中,根据多项研究估计的假阴性和假阳性率现实,NGS方法的FN和其它相比要明显小的多。 看到最后这张汇总的患者丢失示意图,不知道你作何感受。 问题代表着机会和改进空间,问题越大的步骤被优化的可能性也相对越大。不过,除了注意数据的实效性(来自2019年)以外,你或许还需要注意如下几点内容: 如果你对这篇文章感兴趣,欢迎通过邮箱订阅我的 「熊言熊语」会员通讯,我将第一时间与你分享肿瘤生物医药领域最新行业研究进展和我的所思所学所想,点此链接即可进行免费订阅。
🐻:呃,没发财。
👨:那瞎忙啥呢?
🐻:往大了说是精准医疗,研究一些可以检测癌症病人基因组变化的东西,用了之后就能找到针对患者精准的治疗方式。
👨:一种很新的东西?
🐻:算上老美那边,行业从起步到现在已经很多很多年了
👨:那我听说的人得了癌症怎么还都是化疗?
🐻:可能是还没真正普及这种看病方法,而且小地方也有很多不规范
👨:那你不白研究了?
🐻:来,叔,喝一杯
· 分享链接 https://kaopubear.top/blog/2022-03-14-clinical-practice-gaps/